6 淋巴器官和淋巴细胞运输
6.1 二级淋巴器官和淋巴细胞运输
迄今为止,我们已经讨论了获得性免疫和先天免疫的各个因素以及它们是如何相互作用形成一个完整的防御系统的。然而,为了真正理解免疫系统是如何工作的,必须有一张清晰的图片表明所有这些相互作用发生在身体的哪些部位。所以在这一讲,我们着重讨论免疫系统的“地理学”。
实际上,免疫系统防御入侵者有 3 个阶段:危险物的识别、针对入侵者的合适武器的产生以及武器的运输(到攻击位点)。获得性免疫应答的识别阶段发生在所谓的“二级淋巴器官”,包括淋巴结、脾脏和黏膜相关的淋巴组织(MALT)。
你们可能不禁要问:如果这些是二级淋巴器官,那么初始淋巴器官是什么?初始淋巴器官是产生 B 细胞和 T 细胞的骨髓以及 T 细胞接受早期训练的胸腺。
6.1.1 淋巴滤泡
所有二级淋巴器官都有一个共同的解剖学特点——均含有淋巴滤泡。这些滤泡对获得性免疫系统发挥作用是关键的,所以我们有必要花一点时间来熟悉它们。淋巴滤泡的初始形态是“初始淋巴滤泡”——嵌入在富含 B 细胞的二级淋巴器官中滤泡树突状细胞(FDC)的松散网络。所以,淋巴滤泡实际上是位于 B 细胞海洋中的滤泡树突状细胞岛屿。
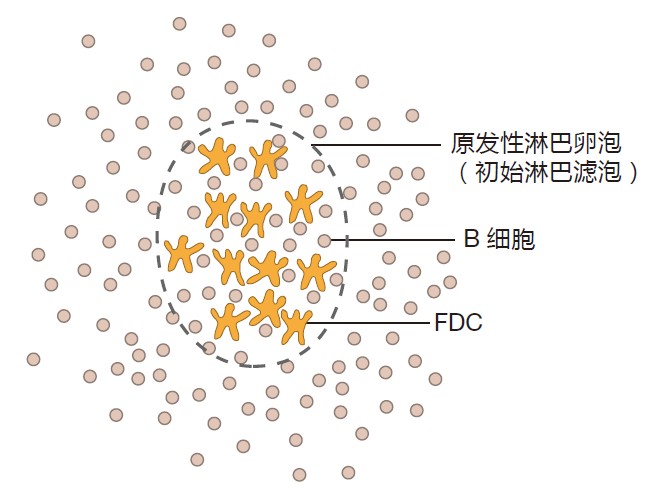
尽管 FDC 具有典型的海星树突状外形,但它又与以前我们谈到的皮肤或黏膜的抗原提呈树突状细胞有较大差别。树突状细胞是骨髓中产生的白细胞,随后迁移到组织中的守卫位置。与此相反,FDC 是常规的老细胞(类似皮肤细胞和肝细胞),随着胚胎的发育在二级淋巴器官中选定了它们的最终位置。实际上,在怀孕的第 6 个月,FDC 就已经位于适当的位置上。滤泡树突状细胞和抗原提呈树突状细胞不仅起源不同,而且这两种海星形的细胞在功能上也有较大差别。
滤泡树突状细胞的功能是将抗原展示给 B 细胞,而树突状抗原提呈细胞的作用是通过 MHC 分子将抗原提呈给 T 细胞。下面介绍它们如何工作。
在感染的早期,补体蛋白结合入侵者后,某些补体调理过的抗原将通过淋巴或血液进入二级淋巴器官。定居在这些器官的滤泡树突状细胞在其表面具有能结合补体片段的受体,因而滤泡树突状细胞能结合并保留调理过得抗原。这样,来源于战斗组织中的抗原修饰了滤泡树突状细胞。在战斗后期,当抗体已产生时,抗体调理过的入侵者也能被滤泡树突状细胞捕获,因为这些细胞有结合抗体分子恒定区的受体,通过捕获大量抗原并紧紧地将它们抓在一起,滤泡树突状细胞以交联 B 细胞受体的方式提呈抗原。
滤泡树突状细胞捕获调理过的抗原,并将其以一种有助于激活 B 细胞的构象形式“介绍”给 B 细胞,那些受体与其同源抗原交联而挂于这些滤泡树突“树”的B 细胞会在淋巴滤泡中停留一会儿,并且在那里增殖以建立其数量群。这种现象一旦发生,“滤泡”就开始增长并形成 B 细胞发育中心,像这样一个活性淋巴滤泡被称为一个“二级淋巴滤泡”或者“生发中心”。在一个生发中心发育的启动过程中,不能(不)过度强调补体调理过的抗原的作用,因为在补体形态缺陷的人体内,淋巴滤泡不能绕过其初始阶段。因此,我们再次看到,为使获得性免疫系统产生反应,先天系统必须首先对即将到来的危险产生应答。
B 细胞生发中心增殖时,变得很“脆弱”。除非它们获得适当的救援相互,否则它们将自杀(通过凋亡而死亡)。幸运的是,二级淋巴器官 T 细胞区内已被激活的辅助 T 细胞迁移至淋巴滤泡以解救这些 B 细胞。被激活的 Th 细胞表达高水平的 CD40L 蛋白,该蛋白能与 B 细胞表面的 CD40 蛋白结合。当一个其受体被抗原交联的 B 细胞接受到这种共刺激信号时,它就暂时从凋亡状态中解救出来,并继续增殖。
B 细胞在生发中心的增殖速率非常惊人——每 6 小时其细胞数将翻倍!这些增殖的 B 不将尚未被激活的 B 细胞挤到一边,在生发中心建立一个称为“暗区”的区域——该区域由于包含了如此多的正在增殖的 B 细胞,在显微镜下,视野是暗的。
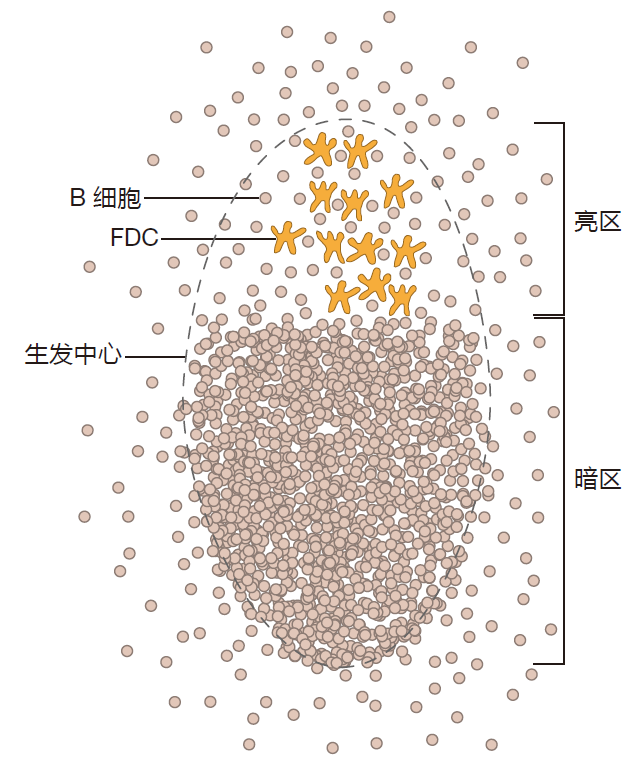
在经过增殖期后,一些 B 细胞“选择”变成浆细胞并离开生发中心,另一些进行体细胞高突变,在每一轮突变后,突变的 BCR 亲和力都要被测试,如果突变的 BCR 对抗原没有足够的亲和力,该 B 细胞将会凋亡而死,随之被生发中心内的巨噬细胞吞噬,相反,如果 BCR 有足够高的亲和力而有效地与 FDC 上的抗原交联,并且如果它们还能从生发中心亮区的被激活 Th 细胞接受到共刺激信号,B 细胞就能从凋亡中解救出来。这就是 B 不在暗区增殖期和亮区检测期之间的循环。有时,在所有这些过程中,B 细胞也能够转换其所产生抗体的类别。人们认为这一过程是在活化的 Th 细胞帮助下,发生在生发中心的亮区。
总之,淋巴滤泡是二级淋巴器官中的特殊区域,在那里,B 细胞渗滤进表面捕获到经过调理抗原的 FDC 的网格中,那些遇到同源抗原并接收到 T 细胞辅助的 B 细胞,就会从死亡中解救出来,这些被解救的 B 细胞即能增殖并进行体细胞高突变和类别转换。显然,淋巴滤泡对于 B 细胞的发育是极其重要的,这就是为什么它们存在于所有二级淋巴器官。
6.1.2 高内皮小静脉
除了脾脏以外,所有二级淋巴器官的第二个解剖学特点是普遍具有高内皮小静脉(HEV)。HEV 之所以如此重要,是因为它们是 B 细胞和 T 细胞从血液进入这些二级淋巴器官的大门。衬于血管内壁的大多数内皮细胞像重叠的瓦片一样紧紧地粘在紧邻它们的细胞上,以防止血细胞损失而进入组织。与之相比,大多数二级淋巴器官中从毛细血管床(毛细血管后微静脉)收集血液的血管内壁被特殊内皮相比所衬,这些特殊的内皮细胞形状更像柱状而非瓦片状。
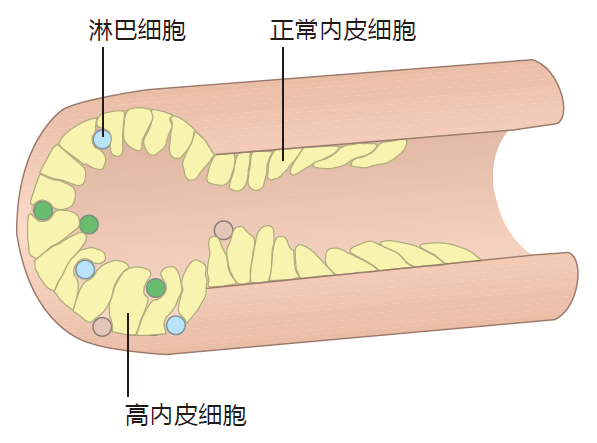
这些长大的细胞就是高内皮细胞。因此,含有高内皮细胞的高内皮小静脉是血管(小静脉)中的一个特别区域。高内皮细胞之间是“点焊连接”而不是黏合在一起,由此,HEV 需之间有足够的空间让淋巴细胞溜掉(蠕动通过)。实际上,蠕动这个词可能用得不是十分恰当,因为在这些高内皮细胞小静脉中淋巴细胞非常有效地离开血液——在高内皮细胞之间,每秒大约有 1 万个淋巴细胞离开血液,进入一个普通大小的淋巴结。
6.1.3 漫游二级淋巴器官
既然你已经熟悉了淋巴滤泡和高内皮小静脉,那么我们准备进一步了解一些二级淋巴器官。在此,我们将了解淋巴结、派尔结和脾脏,在我们探索这些器官时,你需要特别注意“管道”。器官是如何铺设管道的将对其如何行使功能有重要影响。
6.1.3.1 淋巴结
淋巴结是一个“管子工”的梦想之地。该器官有将淋巴液带入淋巴结的输入淋巴管,也有将淋巴液带出淋巴结的输出淋巴管。此外,含有携带有滋养淋巴细胞的血液的小动脉及将血液带出淋巴结的小静脉,如果仔细观看下图,你还可以看到高内皮小静脉。
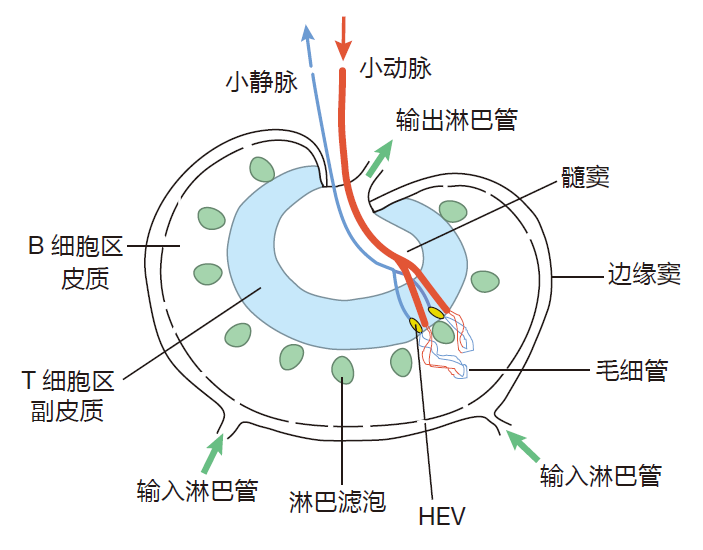
有了这些认识,你知道 T 细胞、B 细胞是怎样进入淋巴结的吗?它们能在血液的推进下穿过高内皮小静脉间的间隙而进入淋巴结。此外,你注意淋巴细胞还有一种进入淋巴结的方式了吗?那就是通过淋巴液。毕竟,淋巴结是“约会酒吧”,它位于淋巴液再次与血液混合的路线上,淋巴细胞主动参与“约会舞会”,通过淋巴液从一个淋巴结被携带到另一个淋巴结,尽管淋巴细胞有两种途径可以进入淋巴结,但是它们只能通过淋巴液离开——它们不能通过高内皮小静脉再回到血液中。
既然淋巴结是淋巴细胞找到它们同源抗原的地方,我们就有必要讨论抗原是如何进入淋巴结的。当驻扎再组织外周的树突状细胞被战斗细胞因子刺激时,它们通过淋巴液离开组织并携带从战场所获得的抗原进入二级淋巴器官,这是抗原进入淋巴结的一种方式——作为“货物”装载于 APC。另外,被补体或抗体调理过的抗原能被淋巴液携带到淋巴结,在那里,调理过的抗原能够被 FDC 捕获,并展示给 B 细胞。当淋巴液进入淋巴结后,经孔渗入到边缘窦(窦是相对于腔的一个假想词),再经过皮质和副皮质,最终进入髓窦,在那里富集,从而经输出淋巴管离开淋巴结。
巨噬细胞衬于边缘窦壁,其职责是清洗淋巴液,因而淋巴结的功能之一就是作为类别滤器。顺便提一下,当外科医生去除身体某器官肿瘤时,他们通常都要检查这些器官引流淋巴液的淋巴结。如果他们在引流淋巴结中找到癌细胞,这就意味着癌细胞已经开始转移到身体的其他部位,邻近的淋巴结是癌细胞转移第一站。
高内皮静脉位于副皮质内,因此当淋巴细胞从血液中到来时,通过淋巴结的副皮质区域。实际上,T 细胞倾向于在副皮质中聚集,通过黏附分子被滞留在那里。T 细胞的这种聚集很有意义,因为在副皮质中也有树突状细胞,而聚集的目的之一就是将 T 细胞与这些 APC 聚集在一起。
当辅助 T 细胞通过淋巴结副皮质时,有可能遇到提呈其同源抗原的树突状细胞。如果是这样,Th 细胞将被激活并开始增殖,增殖会持续几天,大多数新激活的 Th 细胞将会通过淋巴液离开淋巴结,通过血液再循环,并经高内皮小静脉再次进入淋巴结,再循环的过程非常快,通常只需要不到 1 天的时间,但其非常重要。
在获得性免疫系统产生抗体之前,必须要具备 4 个主要条件:APC 提呈抗原给 T 细胞;Th 细胞身体识别被提呈的抗原;FDC 展示调理过的抗原以及 B 细胞受体识别抗原。在感染早期,这些因素并不多,原初 B 细胞和 T 细胞随机地在二级淋巴器官循环,寻找与其受体相匹配的配体。因此,识别特定抗原的稀少的 Th 细胞达到本身个体很小的淋巴结,而与此同时,对同一个抗原有特异性的稀少的 B 细胞也进入这个淋巴结,这种概率是相当小的。然而,如果激活的 Th细胞首先增殖,增加其数目,然后再循环到大多数淋巴结和其他二级淋巴器官,这些激活的 Th 细胞得到扩散,使得它们有较大的可能性遇到那些需要其帮助的稀少的 B 细胞。
当再循环的 Th 细胞进入正在提呈其同源抗原的淋巴结时,它们将被再刺激,一些再刺激的 Th 细胞将更多地增殖,并再次循环以进一步提供其辅助能力,另一些再刺激的 Th 细胞将移到淋巴结的淋巴滤泡对需要帮助的 B 细胞提供帮助,此外还有一些将离开血液以提供细胞因子帮助再组织中战斗的武士。
如果杀伤性 T 细胞找到被辅助 T 细胞“特许”的由树突状细胞提呈的同源抗原,它们会在淋巴结副皮质中被激活。一旦被激活,CTL 就增殖并进入再循环,其中一些再次进入二级淋巴器官并开始其循环,而另一些则离开感染部位的血液去杀死病毒感染的细胞。
B 细胞也参与了激活、增殖、循环和再刺激的周期,但对于原初 B 细胞首先在哪里激活及怎样被激活仍未明了。最新证据表明,已经由遇到 FDC 展示其同源抗原的 B 细胞将迁移到淋巴滤泡边缘,在那里它们遇到已经从副皮质迁移过来的激活的 T 细胞。在这次“会面”期间,B 细胞首先接收其激活必需的共刺激,然后,B 细胞和 T 细胞进入淋巴滤泡,并且 B 细胞增殖。许多新产生的 B 细胞通过淋巴液离开淋巴滤泡,有些形成浆细胞,驻扎在脾和骨髓中,并大量产生抗体;另一些随着淋巴和血液再循环,再次进入淋巴器官,结果,活化的 B 细胞可以扩散到许多二级淋巴器官,在那里,如果它们在淋巴滤泡中再次被刺激,它们就增殖得更多,并进行体细胞高突变和类别转换。
B 细胞在生发中心中的急剧活化,通常需要大约三周以上的时间。此时,入侵者已被击退,大多数被调理过的抗原被 B 细胞从树突状细胞中“拾取”。大多数B 细胞将离开滤泡或者在那里死亡,而那些曾经是生发中心的区域,将会看起来更像是初级淋巴滤泡。
从以上讨论可以清晰看出,淋巴结是一个高度组织化的地方,那里有包含APC、T 淋巴细胞和 B 淋巴细胞的特殊区域。但是,在淋巴结内,APC 和淋巴细胞怎样知道应该去哪里的?最近几年,免疫学家一直在寻求该问题的答案,它们通过实验已经发现一种特殊类型的细胞因子——趋化因子(化学趋化细胞因子的简称)。尽管还有一些细节未弄清楚,但现在已知道的是,APC 和淋巴细胞在它们发育的不同阶段表达不同组合的受体,不同组合的受体与趋化因子蛋白家族的不同成员相匹配。例如,当树突状细胞在组织外围被激活后,它们开始表达趋化因子受体CCR7。这种受体可以检测到树突状细胞与 T 不会面的淋巴结区域中细胞所产生的趋化因子。因此,一旦树突状细胞到达淋巴结,它们就会被趋化因子的“气味”所吸引而到达正确的位置。同样,淋巴结中的FDC产生称为 BLC的趋化因子。B 细胞表达该趋化因子的受体,并可被吸引至FDC展示调理抗原的淋巴结区域。在淋巴结 T 细胞区内被树突状细胞激活的 Th 细胞也表达BLC受体,当这些受体检测到FDC产生的BLC时,激活的 T 细胞将会大胆进入淋巴结的 B 细胞区,帮助 B 细胞激活。
当然,人体细胞不能像某些细菌一样装备小型推进器,因此,它们不能游向趋化因子的方向。人体细胞所能做的只能是“蠕动”。一般而言,能感觉到有最大浓度细胞因子的细胞末端伸向趋化因子源,另一端却缩进。
总之,淋巴结具有淋巴滤器的作用,来自感染组织的抗原,无论是否被树突状细胞搭载,均被淋巴结拦截,这些淋巴结可以为抗原、APC、T 细胞和 B 细胞提供一个相对集中而有组织的环境。在该环境中,原初 B 细胞和 T 细胞能被激活,而有经验的 B 和 T 细胞能被再次刺激。在淋巴结中,原初 B 细胞和 T 细胞成熟为效应细胞——B 细胞产生抗体,Th 细胞提供细胞因子帮助和 CTL 杀伤被感染细胞。简而言之,淋巴结能做所有这些事。
众所周知,引流感染部位的淋巴结倾向于膨胀。例如,如果你患上了上呼吸道感染(如流感),颈部的淋巴结可能会肿大,部分原因是由于淋巴结中淋巴细胞的增殖,此外还由于在活化的淋巴结中,辅助 T 细胞产生的细胞因子募集额外的巨噬细胞,可能导致髓窦堵塞的倾向。结果导致液体滞留在淋巴结内,引起更进一步的肿胀。当入侵者被击溃后,就不再有足够的抗原来保持 B 细胞和 T细胞的激活状态。此时,大多数 B 细胞和 T 细胞由于衰竭或者缺乏刺激而死亡,淋巴结的肿胀也因此而消退。
6.1.3.2 派尔结
早在17世纪晚期,瑞士解剖学家 Johann Peyer观察到有平滑细胞小结被包埋在衬于小肠的绒毛细胞间,我们现在知道,这些“派尔结”是黏膜相关淋巴组织(MALT)的一类,它作为二级淋巴器官发挥作用。这是一张显示派尔结基本特征的图。
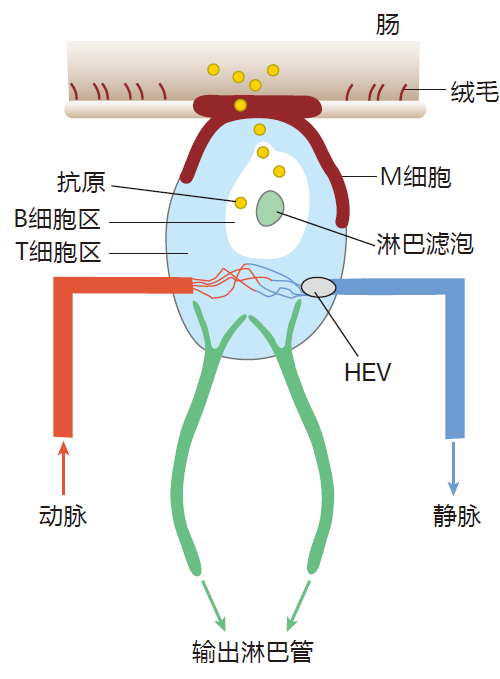
派尔结内有高内皮小静脉,淋巴细胞通过它从血液进入派尔结。当然,也还有将淋巴液从组织中引流出的输出淋巴管。然而,不同于淋巴结,派尔结没有将淋巴液带入结内的输入淋巴管。如果没有输入淋巴管,抗原是如何进入这一二级淋巴器官的呢?
你注意到位于派尔结顶部的光滑细胞了吗?这些细胞上没有“毛发”,被称为M 细胞,它专职将抗原从小肠内部运输至 M 细胞下面的组织内。为了达到这一目的,M 细胞将肠抗原包入与巨噬细胞的吞噬体大体相似的被称为内体的囊中。
这些内体通过 M 细胞运输,随后又被M细胞将其内容物吐到细胞的另一侧。因此,淋巴结从淋巴液中获取抗原,派尔结却从小肠中获取抗原并且这些运输抗原的过程均由M细胞来完成。
M细胞收集的抗原能被引流自派尔结的淋巴液携带至淋巴结。如果这些收集的抗原被补体或者抗体调理过,它就可被M细胞下面的淋巴滤泡中的FDC捕获。
实际上,除了获取抗原不同于寻常的方法外,派尔结和淋巴结非常相似,都具有引进T细胞和B细胞的高内皮小静脉和供这些细胞聚合的特殊区域。
最近发现,M细胞对运输的抗原有相当的选择性,M细胞并不一点一点的啜饮肠道中的任何东西。这些细胞仅运输那些能与M细胞表面分子结合的抗原。
这种选择具有完美的意义。M细胞和派尔结的目的就是帮助启动针对侵入肠道病原体的免疫反应,但对病原体来说,棘手的是它必须衬于肠内的细胞并侵入其下面的组织。因此,微生物造成危害的最低条件是它能结合在肠细胞表面。相反,我们吃的大多数食物在消化的各个阶段没有结合任何东西就穿过肠道,因而,通过忽略所有“非结合物”,M细胞就避免了因无关的食物抗原而激活免疫系统,从而使派尔结着重对付那些潜在的病原体。
6.1.3.3 脾脏
我们所要了解的最后一个二级淋巴器官是脾脏。它位于动脉和静脉之间,并作为血液滤器而发挥作用。与派尔结一样,脾脏没有将淋巴液带入其内的淋巴管。
然而,不同于派尔结和淋巴结只能通过高内皮小静脉才能将血液的B细胞和T细胞带入,脾脏更像一个“开放家庭集会”,在这血液中所有的东西被邀请进来。
以下是组成一个脾脏滤器单元的示意图。
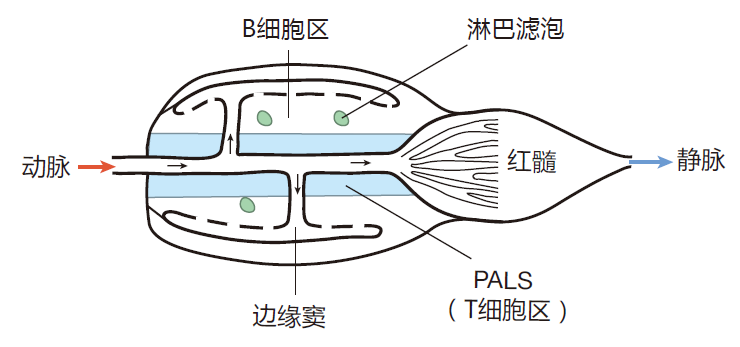
血液从脾动脉进入,并向外流向边缘窦,继而渗透入整个脾脏,最后进入静脉。巨噬细胞衬于边缘窦内,通过吞噬细胞碎片和外源入侵者而净化血液。当原初B细胞和原初T细胞一起流动时,它们会停留在不同的区域。T细胞位于环绕于中心小动脉的动脉周围淋巴鞘(PALS)的区域;B细胞位于PALS和边缘窦之间的区域。一旦被PALS内的APC激活,辅助T细胞就移入淋巴滤泡,以帮助已经识别其同源抗原的B细胞,这在前面已有所讨论。
6.1.4 二级淋巴器官的合理性
迄今为止,我相信你已经理解造物主在做什么。每一个二级淋巴器官都是战略性地被安置来阻拦从不同途径进入身体的入侵者。如果皮肤被刺破进而引起组织感染,在引流这些组织的淋巴结中就产生了免疫反应。如果你除了被污染的食物,小肠内的派尔结就产生免疫反应。如果你被血源性病原体侵犯,你的脾脏过滤它们并启动免疫反应,如果入侵者通过呼吸道侵入,另一套包括扁桃体在内的二级淋巴器官就在那里保护你。
二级淋巴器官不仅被战略性放置,而且它们提供了一套有助于武器动员的装置,这些武器适宜对付最可能遇到的入侵者。具体的机制目前还不清楚,但普遍认为,不同的二级淋巴器官其细胞因子环境也不同。器官中固有的细胞因子与APC提供的共刺激分子共同决定免疫反应的特征。例如,派尔结专职产生能分泌Th2型细胞因子的Th细胞和分泌IgA抗体的B细胞,是抵抗肠道入侵者的完美武器。相反,如果细菌从趾伤口入侵,膝下淋巴结产生的Th1细胞和分泌的IgG 抗体的B细胞是防御细菌入侵的理想武器。
前面我曾把二级淋巴器官描绘成“约会酒吧”,在二级淋巴器官中,T细胞、B细胞和APC“混在一起”。实际上情况比这更好些,因为二级淋巴器官确实更像“婚介机构”。当男士或者女士通过婚介机构找各自的配偶时,他们从填写调查表开始,调查表中信息包括他们的背景和所要寻找的目标,然后,计算机搜寻所有的调查表并将可能适合的男士和女士配对,因为已被预先分检过,通过这种方法,男士找到适合他的女士机会大大增加,这种预选形式也存在二级淋巴器官中,其具体过程如下。
在我们的讨论中,我们已经注意到二级淋巴器官被“分隔”,原初B细胞和原初T细胞有各自独立的领域。当成千上万的Th细胞通过二级淋巴器官的T细胞区时,只有少部分(即那些同源抗原位于T细胞区的APC展示的)细胞会被激活,那些没有找到同源抗原的Th细胞就离开了二级淋巴器官并继续循环,只有在T细胞区激活的“幸运”Th细胞会增殖,然后迁移至发育中的生发中心,为B细胞提供辅助,这具有完美的意义:如果让那些无用的、未被激活的Th细胞进入B细胞区域,只会使一切变得乱七八糟的并将降低合适的Th细胞和 B细胞在一起的概率。
同样,大量B细胞进入二级淋巴器官的B细胞区,寻找由FDC展示的同源抗原,只有少部分会找到能被其受体识别的抗原,余下的大部分将继续行进。这些稀少的B细胞停留在二级淋巴器官,并与激活的Th细胞相互作用。通过对二级淋巴器官各自区域的淋巴细胞预选,造物主就确保当 Th细胞和B细胞最终相遇时,将有最大机会找到它们的“配偶”——就像婚介机构进行的一样。
尽管在Th细胞和B细胞会面之前,对其进行预选是一个很好的主意,但对二级淋巴器官内淋巴细胞分门别类还是引出一个问题。激活的Th细胞对原初B细胞的激活涉及细胞与细胞间的相互接触,即Th细胞上的 CD40L蛋白结合到B细胞上的 CD40蛋白。然而,当CD40L和 CD40相互作用发生时,参与的 CD40L蛋白快速被带入Th细胞内部,很快,Th细胞表面没有足够的 CD40L 为B细胞提供帮助,结果Th 细胞“耗尽汽油”,为了“再加油”,Th 细胞必须再刺激。如果发生再刺激,更多的CD40L蛋白将产生并迁移至 Th细胞表面,细胞就能再发挥其作用。然而,问题就在于当 Th 细胞“耗尽汽油”后,它并不再定居于最初为其提供刺激的 APC 所处的 T 细胞区,那么,Th 细胞是怎样获得再刺激呢?
当 B 细胞结合于 FDC 所展示的同源抗原时,抗原就被带入B细胞,剪切成片段,并且由B细胞表面的 MHCⅡ类分子提呈,一旦B细胞被激活,将在其表面表达B7分子。因此,激活的B细胞就具备了作为 APC 发挥作用并再刺激已“耗尽汽油”的辅助T细胞的所有条件。因此在淋巴滤泡中,Th细胞和B细胞共舞,在那里Th细胞提供了激活B细胞所需的共刺激(CD40L),而B细胞则为T细胞“再充电”提供了提呈的抗原和必需的共刺激(B7)。
6.1.5 淋巴细胞运输
到目前为止,我们已经讨论了 T 细胞和B细胞在二级淋巴器官相遇而激活的事件,但我们并没有更多地谈到这些细胞如何知道要去哪?免疫学家称这一过程为“淋巴细胞运输”。在人体中,大约每天有 5000 亿个淋巴细胞从血液流经各种二级淋巴器官,然后又流回血液,进行周而复始的循环。然而,这些细胞并不只是四周游荡,它们遵循一个小心谨慎被配合运输的模式,以期最大限度地增加其遇到入侵者的机会。重要的是,原初淋巴细胞和有经验的淋巴细胞的运输模式是不同的。首先看一下原初 T 细胞的运输。
T 细胞来源于骨髓,并在胸腺中受训,当它们从胸腺中出来时,原初 T 细胞表面有作为“世界范围的通行证”的细胞黏附分子的混合物,因而可以被运输至任一个二级淋巴器官。例如原初 T 细胞表面有 L-选择素分子,能结合到它的粘附伴侣 GlyCAM-1 上,而 GlyCAM-1 存在于淋巴结高内皮小静脉,这是原初 T 细胞的“淋巴结通行证”。原初 T 细胞也表达整合素α4β7,它的粘附伴侣是存在于派尔结和引流肠附近淋巴结(肠系膜淋巴结)的高内皮小静脉中 MadCAM-1,所以这种整合素是原初 T 细胞到达肠区的通行证。通过装备这些黏附分子,原初T细胞就可以在所有的二级淋巴器官循环。这非常有意义:T细胞受体的基因是通过基因片段的随机选择过程而被组装的,因此一个特定的原初T细胞不会事先知道会在身体哪个部位遇到其同源抗原。
在二级淋巴器官中,原初 T 细胞穿过T细胞区内抗原提呈细胞富含区,如果在那里没有遇到被展示的同源抗原,它们就直接(如在脾脏)或者通过淋巴再次进入血液,继续循环,每12至24小时完成一次循环周期。一个原初T细胞可以持续这种循环很长一段时间,但大约6周后,如果T细胞没有遇到由MHC提呈的同源抗原,它将会由于凋亡,高度孤独而失望地死去。相反,那些幸运的能找到其抗原的原初T细胞会在二级淋巴器官中被激活,这时,它们就变成“有经验”的T细胞。
有经验的T细胞也携带通行证,但因为在激活期间,T细胞表面的某些黏附分子表达增加,另一些减少,其携带的通行证是“限制性通行证”。这种黏附分子表达的调控不是随机的,而是有计划的。实际上,激活T细胞表达的细胞黏附分子取决于这些T细胞在何处被激活。例如,在派尔结内被激活的T细胞表达高水平的整合素α4β7(肠特异的整合素)和低水平的 L-选择素(更普通的叫法是高内皮静脉黏附分子),因此在派尔结内被激活的 T 细胞更倾向于返回派尔结,这样,当激活的 T 细胞再循环时,它们通常离开血液并再次进入与遇到抗原时相同类型的二级淋巴器官。这些限制性的运输模式是相当具有逻辑性的。毕竟,如果肠道被侵袭了,让有经验的辅助T细胞再循环至膝下淋巴结当然是毫无意义的,此时需要的是那些有经验的辅助T细胞直接回到肠道,再次被刺激并提供帮助。因此通过限制性通行证装备激活的T细胞,造物主可以确保这些细胞将回到它们最有可能遇到其同源抗原的地方——派尔结、淋巴结或扁桃体。
当然,也不能让T细胞总是不停地循环,也需要它们从感染部位的血液离开,以杀死病毒感染的细胞或者提供细胞因子以增加免疫反应,并从血液补充更多的战士,为了完成这一过程,有经验的T细胞携带着指导它们离开感染部位血液的额外通行证(黏附分子)。这些T细胞运用与中性粒细胞离开血液进入炎症组织时相同的“滚动、嗅闻、停止和离开”讲述。例如,从黏膜获取有经验的T细胞表达整合素αEβ7,当它的粘附伴侣——地址素分子表达在发炎的黏膜血管,于是这些受过训练能对付黏膜入侵者的T细胞触发寻找被感染的黏膜组织,在这些组织中,由前线的“士兵”释放趋化因子,通过与活化过程中T细胞表面出现的趋化因子受体结合,以帮助引导T细胞到达战场。
总之,原初T细胞有允许它们访问所有二级淋巴器官的通行证,但不能访问炎症部位。这种运输模式使整个原初T细胞群体可能与已经进入身体任何部位的入侵者在二级淋巴器官相互接触,大大增加了原初T细胞被激活的可能性。
原初T细胞没有携带战场通行证的原因在于,在被激活以前,它们不能在那里以任何方式做任何事。
与原初T细胞相对,有经验的T细胞有限制通行证可以使它们返回到与当初它们获得经验时相同类型的二级淋巴器官。通过优先再循环到它们最初遇到抗原的那种类型器官中,T细胞就更有可能被再刺激,或者找到已经遭遇相同入侵者并需要它们帮助的CTL和B细胞。
激活的T细胞也有允许它们离开被感染部位血液的通行证,从而使得CTL杀伤被感染的细胞,Th细胞提供合适的细胞因子指导这场战斗,这种奇妙的“邮政系统”是由黏附分子和趋化因子组成的,可以确保将合适的武器运送到所需要的部位。
B细胞的运输基本上与T细胞相似。类似原初T细胞,原初B细胞也有通行证可以允许它们到达二级淋巴器官的所有范围,然而,有经验的B细胞并不像有经验的T不一样倾向于迁移,它们大多数仅仅定居在二级淋巴器官和骨髓中,产生抗体,然后让这些抗体去旅行完成任务。
6.1.6 母亲为什么要亲吻婴儿
你是否知道为什么母亲要亲吻她们的婴儿?这是她们一定会做的事情。大多数圈养动物也亲吻它们的婴儿,尽管在这种情况下,我们多称之为舔。让我来告诉你为什么它们要这么做吧。
新生儿的免疫系统发育不完善。实际上,直到出生后几个月,IgG才会产生。
幸运的是,母亲血液的IgG能通过胎盘进入胎儿血液,因此新生儿可以从母体那里获得这种“被动免疫”而克服不能产生IgG的情况。新生儿也能接受另一种类型的被动免疫——从母乳中获取IgA抗体。在哺乳过程中,血浆B细胞迁移至煤气的乳房,产生 IgA分泌到乳汁中,这种作用很伟大,因为婴儿遇到的大多数病原体是通过口或鼻进入肠道,并进而引起腹泻。通过摄入富含IgA抗体的母乳,婴儿的消化道可以被抗体所覆盖,从而阻隔这些病原体。
然而,你会意识到,在母亲的一生中,她会暴露于许多不同的边有人,因而她们所产生的大多数针对这些病原体的抗体对婴儿是没有用的。例如,母亲可能会具有能识别引起单核细胞增生的EB病毒的抗体,但直到婴儿开始成年,他们才有机会接触该病毒。如果母亲能够提供能识别婴儿遇到的那些病原体的抗体,而不是提供对婴儿完全没用的抗体,这不是很好吗?是的,事实的确如此。
当母亲亲吻婴儿时,她就对婴儿脸部的病原体进行“取样”——这些病原体正是婴儿将摄入的。由母亲的二级淋巴器官(如扁桃体)接纳了这些病原体,然后对这些病原体特异性的记忆B细胞就会再次被刺激,这些激活B细胞随之移到母亲的乳房,在那里产生大量的抗体,而这些抗体恰好是婴儿所需要的。


